השמנה
מנהלי קהילה
מובילי קהילה
ה-FDA אישר מכשיר ראשון מסוגו לטיפול בהשמנה
מנהל המזון והתרופות האמריקאי אישר מכשיר המושתל בגוף ומעביר זרמים חשמליים לקיבה לטיפול בהשמנה
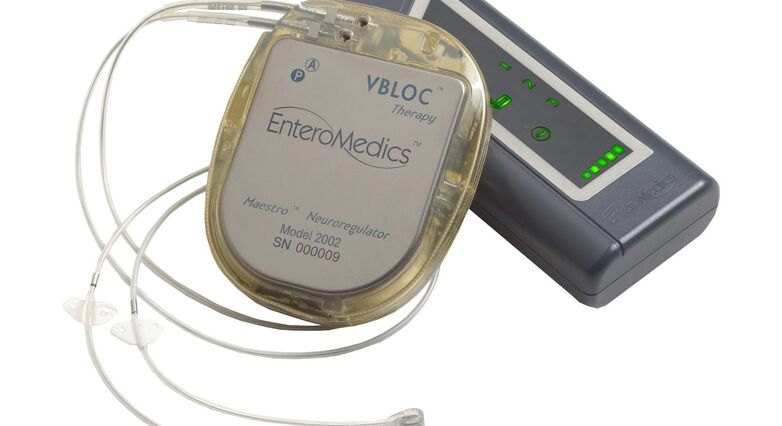
מנהל המזון והתרופות האמריקאי אישר אתמול (ד') מכשיר חדשני המכונה 'מאסטרו' (Maestro Rechargeable System) של חברת EnteroMedics לטיפול בהשמנת יתר.
מדובר במכשיר הראשון שפועל על המסלול העצבי שבין המוח לקיבה השולט בתחושות של רעב ושובע. המכשיר מושתל בניתוח וניתן להטעין אותו, לכבות אותו או לשנות את הפעילות שלו באמצעות מתאם חיצוני.
המאסטרו אושר לשימוש בבני 18 ומעלה שלא הצליחו לרדת במשקל בעזרת תוכנית הרזיה רגילה ויש להם BMI (מסת גוף) של 40 עד 45 או BMI של 35 ומעלה יחד עם לפחות מצב רפואי אחד הקשור להשמנה, כמו סוכרת סוג 2 או יתר לחץ דם.
מערכת המאסטרו מורכבת ממכשיר נטען המפיק זרמים חשמליים, חוט חשמל המוביל את הזרם ואלקטרודות המושתלות בבטן. היא פועלת באמצעות שליחת זרמים חשמליים לסירוגין לעצב התועה (ואגוס) בבטן, המעורב בוויסות ריקון הקיבה ומאותת למוח על כך שהקיבה מלאה או ריקה. בהודעה שפרסם ה-FDA מוסבר כי ידוע שהגירוי החשמלי חוסם את הפעילות העצבית בין המוח והקיבה, אך המנגנון הספציפי לירידה במשקל עקב השימוש במכשיר אינו ידוע.
הבטיחות והיעילות של המאסטרו הוערכו במחקר קליני שכלל 233 מטופלים עם BMI של 35 ומעלה, מתוכם 157 טופלו במאסטרו ו-76 טופלו במאסטרו שלא הופעל באמת (טיפול דמה) והיוו קבוצת ביקורת. במחקר נמצא כי לאחר 12 חודשים הקבוצה שטופלה במכשיר איבדה 8.5% יותר מהמשקל העודף בהשוואה לקבוצת הביקורת. כמחצית (52.5%) מהנבדקים שטופלו במכשיר ירדו לפחות 20% מהמשקל העודף ו-38.3% ירדו לפחות 25% מהמשקל העודף. בין תופעות הלוואי שדווחו במחקר היו בחילה, הקאות, צרבת, גיהוקים, בעיות בליעה, כאב וסיבוכים של הניתוח בו הושתל המכשיר.
כחלק מתנאי האישור, יצרנית המאסטרו נדרשת לערוך מחקר שיעקוב אחר לפחות 100 מטופלים במשך חמש שנים, שיספק מידע נוסף על יעילות ובטיחות המכשיר בטווח הארוך.






















pfs1
233 משתתפים - זה לא בדיוק מחקר עומק [ או רוחב].
סביר להניח שגם מבחינת משך הזמן לקחו את המינימום שיכלו.
רוויה
לא דווח לכמה מהנבדקים היו את תופעות הלוואי ומה הייתה רמתם.